EMA a autorizat utilizarea în caz de urgență a pastilei anti-Covid de la Pfizer, Paxlovid / Care sunt beneficiile și contraindicațiile tratamentului
Agenția Europeană a Medicamentului (EMA) a aprobat utilizarea în caz de urgență în Uniunea Europeană a pastilei anti-Covid de la Pfizer, care nu a primit încă autorizație completă de introducere pe piață, relatează AFP.
„Medicamentul, care nu este încă autorizat în UE, poate fi utilizat pentru a trata adulții cu Covid-19 care nu au nevoie de oxigen suplimentar și care prezintă un risc crescut de a dezvolta o formă severă a bolii”, a spus EMA într-un comunicat.
„EMA a emis acest aviz pentru a sprijini autoritățile naționale care pot decide cu privire la o posibilă utilizare timpurie a medicamentului”, în condițiile în care continentul se confruntă cu o creștere a numărului de cazuri.
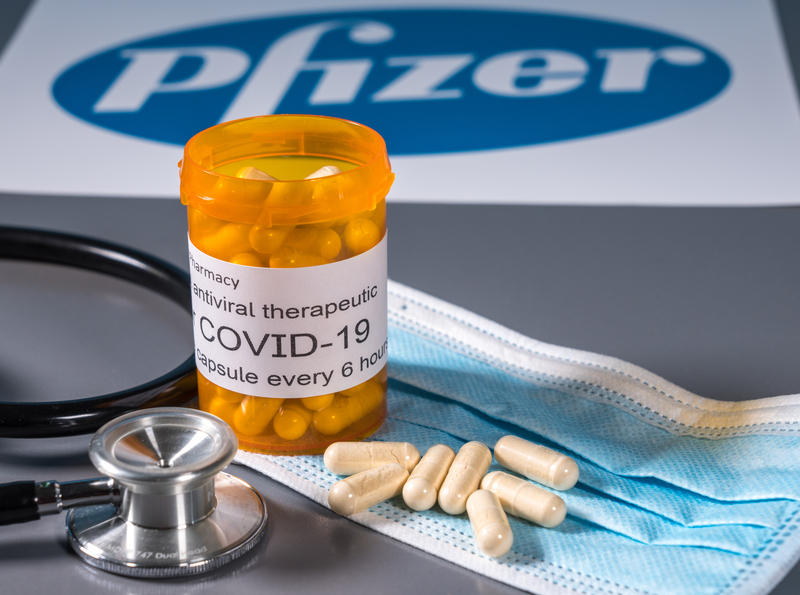
Gigantul farmaceutic a anunțat la începutul acestei săptămâni că pilula sa anti-Covid a redus spitalizările și decesele la persoanele cu risc cu aproape 90% atunci când aceasta este luată în primele zile după apariția simptomelor.
Pastila, denumită Paxlovid, ar trebui să rămână eficientă împotriva Omicron conform testelor de laborator, a mai anunțat Pfizer.
Beneficiile și contraindicațiile Paxlovid
Recomandarea EMA se bazează pe rezultatele intermediare ale studiului principal la pacienții care nu sunt spitalizați și care nu sunt vaccinați care se confruntă cu boală simptomatică, dar care prezentau riscul de a dezvolta o formă severă a bolii.
Aceste rezultate indică faptul că Paxlovid „a redus riscul de spitalizare și deces atunci când tratamentul a fost administrat în decurs de 5 zile de la debutul simptomelor”, iar tratamentul ar trebui prelungit pe cinci zile.
Antiviralele acționează prin reducerea capacității unui virus de a se replica, încetinind astfel boala.
Sunt așteptate cu nerăbdare pentru că sunt ușor de administrat și pot fi luate acasă cu un pahar cu apă.
Tratamentul nu este recomandat în timpul sarcinii și la persoanele susceptibile de a rămâne însărcinate. De asemenea, alăptarea trebuie întreruptă în timpul tratamentului.
Cele mai frecvente efecte secundare au fost tulburări ale simțului gustativ, diaree și greață.
EMA a lansat, de asemenea, o evaluare accelerată a tratamentului pe 13 decembrie 2021 pentru o posibilă cerere de autorizație de introducere pe piață.
EMA a emis o autorizație similară de utilizare în caz de urgență pentru o pastilă de la rivalul Pfizer, Merck.
Agenția Europeană a Medicamentelor a aprobat joi alte două tratamente anticovid, respectiv sotrovimab, produs de GlaxoSmithKline şi compania Vir Biotechnology, și Kineret, creat de producătorul suedez de medicamente pentru boli rare Sobi.