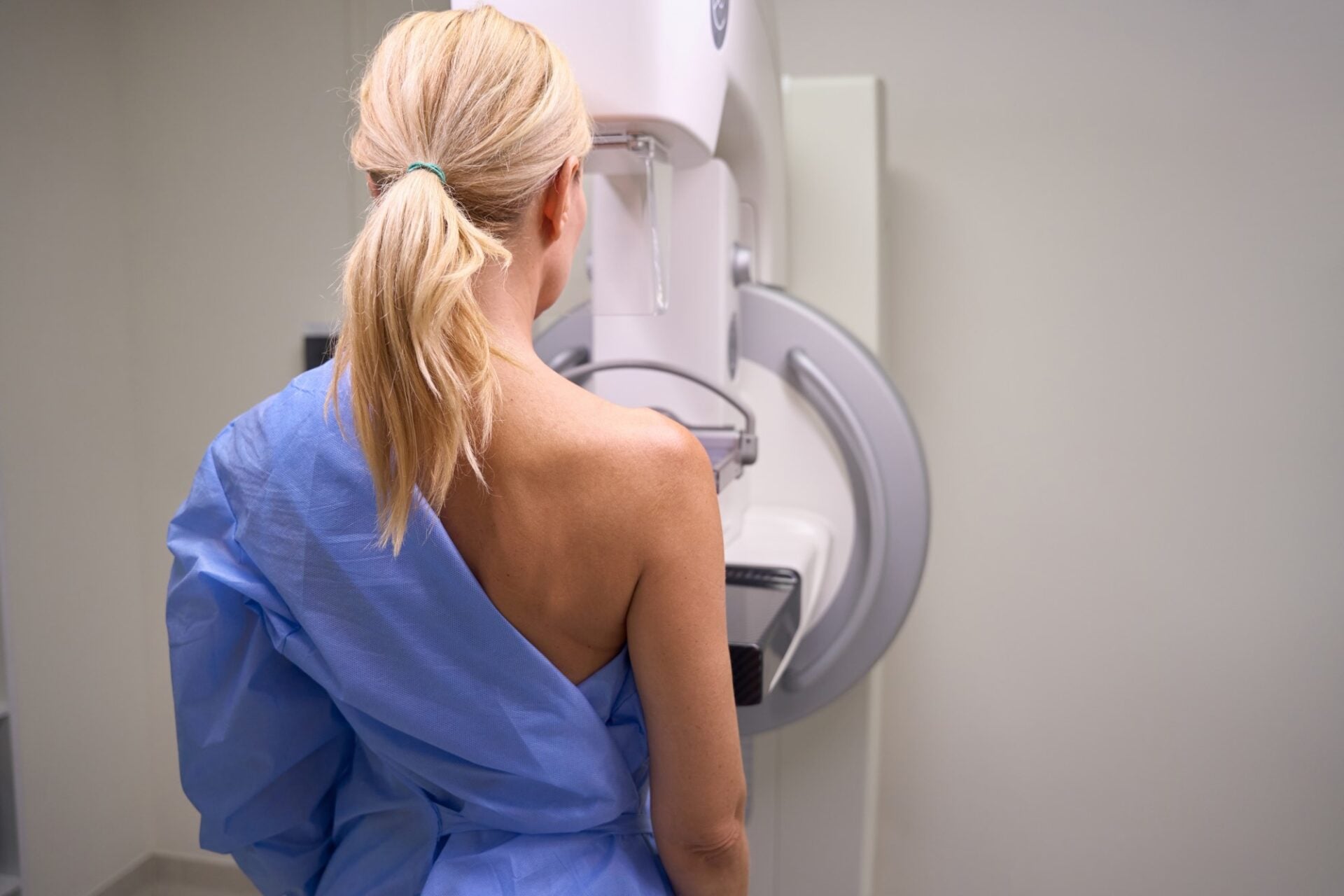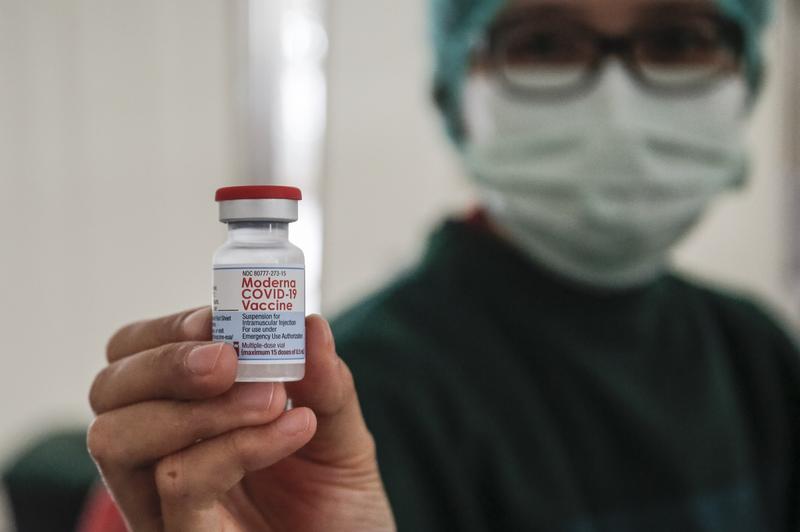
Moderna a cerut autorizarea în UE a vaccinului său anti-Covid pentru copiii cu vârste între 6 și 11 ani, deși multe state întrerup administrarea acestui ser la persoane sub 30 de ani
Compania Moderna a cerut marți autorizarea europeană a vaccinului său anti-Covid pentru copiii cu vârsta cuprinsă între 6 și 11 ani, la câteva săptămâni după ce a amânat o cerere similară la autoritățile de reglementare din SUA, relatează Reuters.
În iulie, Uniunea Europeană autorizase vaccinul pentru adolescenți cu vârsta cuprinsă între 12 și 17 ani, dar mai multe țări, inclusiv Suedia, au întrerupt utilizarea vaccinului pentru persoanele sub 30 de ani din cauza efectelor secundare rare precum miocardita.
Moderna a declarat la sfârșitul lunii octombrie că autoritatea de reglementare a medicamentelor din SUA are nevoie de mai mult timp pentru a-și finaliza evaluarea vaccinului pentru utilizarea la grupa de vârstă 12-17 ani, deoarece studiază riscul unui tip de inflamație a inimii, numit miocardită, după vaccinare.
Producătorul de medicamente a amânat cererea autorizării în SUA pentru copiii cu vârste cuprinse între 6 și 11 ani, în timp ce FDA își finalizează revizuirea privind utilizarea vaccinului la grupa de vârstă 12-17 ani.
La începutul lunii octombrie, compania a declarat că vaccinul său a generat un răspuns imun puternic la copiii cu vârsta cuprinsă între 6 și 11 ani și că intenționează să trimită datele autorităților de reglementare globale în curând.
Moderna a declarat marți că a solicitat Agenției Europene pentru Medicamente utilizarea unei doze de 50 de micrograme de vaccin la copii, jumătate din doza folosită în vaccinurile pentru adulți.